编者按:第23届全国临床肿瘤学大会暨2020年CSCO学术年会于9月19日~26日在北京等五地以线上+线下的形式举行。在9月21日的乳腺癌专场上,北京大学人民医院王殊教授就《早期三阴性乳腺癌新辅助免疫治疗——机遇和挑战》做了精彩报告。肿瘤瞭望特将讲课内容及其对三阴性乳腺癌治疗的观点进行了整理,供读者学习。
新辅助治疗越来越多的应用于乳腺癌患者的治疗中,尤其对于三阴性乳腺癌(TNBC)和HER2+乳腺癌患者,新辅助治疗药敏平台的筛选作用可以指导后续治疗。但与HER2+乳腺癌相比,由于缺少相应靶点,TNBC传统的新辅助化疗效果已经趋于瓶颈,免疫检查点抑制剂的出现给TNBC的新辅助治疗提供了更多的治疗机会。
晚期TNBC患者免疫治疗的数据主要来自于KEYNOTE系列研究和IMpassion 130研究,在新辅助治疗领域,2020年ESMO大会报道了IMpassion 031的研究结果,该研究旨在评估阿替利珠单抗(Atezolizumab)联合化疗在早期TNBC新辅助治疗中的疗效和安全性,主要研究终点是病理完全缓解(pCR),定义为ypT0/is ypN0。结果显示与对照组相比,阿替利珠单抗联合化疗,pCR的绝对获益高达16.5%(57.6% vs 41.1%,P=0.0044),次要研究终点PD-L1阳性患者与ITT人群pCR获益一致(58.8% vs 34.8%,P=0.021)。
与晚期TNBC免疫治疗的IMpassion130研究结果不同,IMpassion031研究中即使是PD-L1阴性患者,其pCR率仍然有获益的趋势(47.7% vs 34.4%)。同时,为了解新辅助免疫治疗获得的近期疗效能否转化为远期生存的获益,该研究还做了长期生存的探索,不管是EFS、DFS还是OS,都看到新辅助免疫治疗获益的趋势,但是目前长期生存的数据尚不成熟,期待后续随访结果的公布。
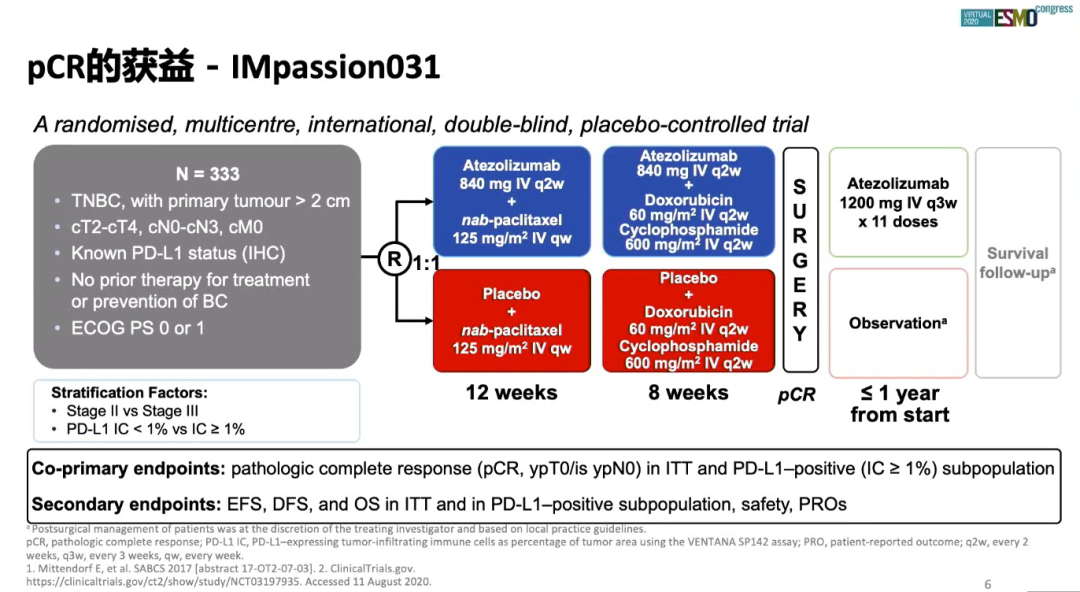
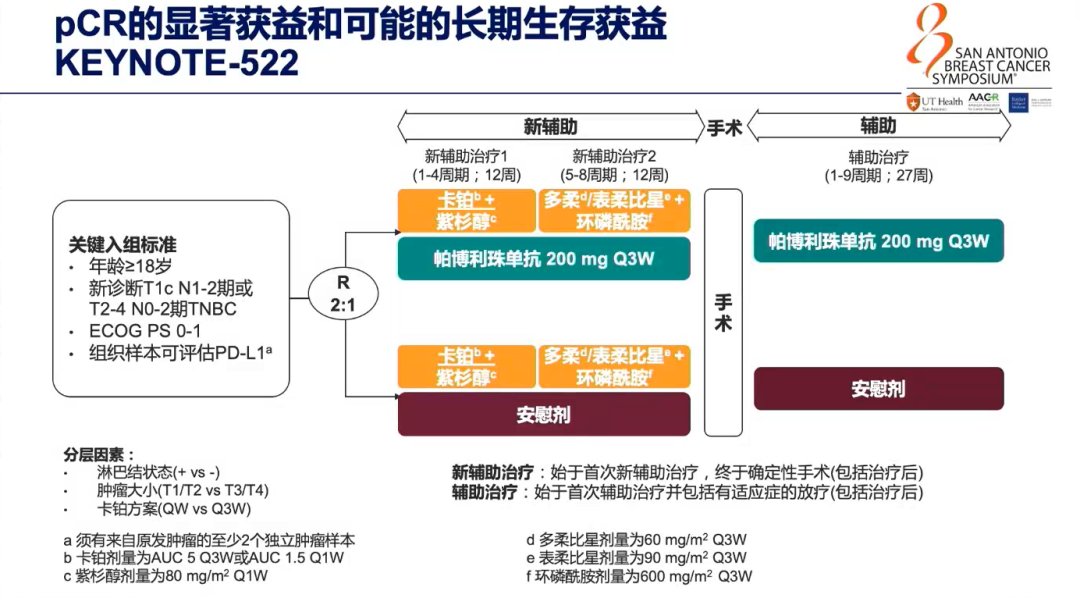
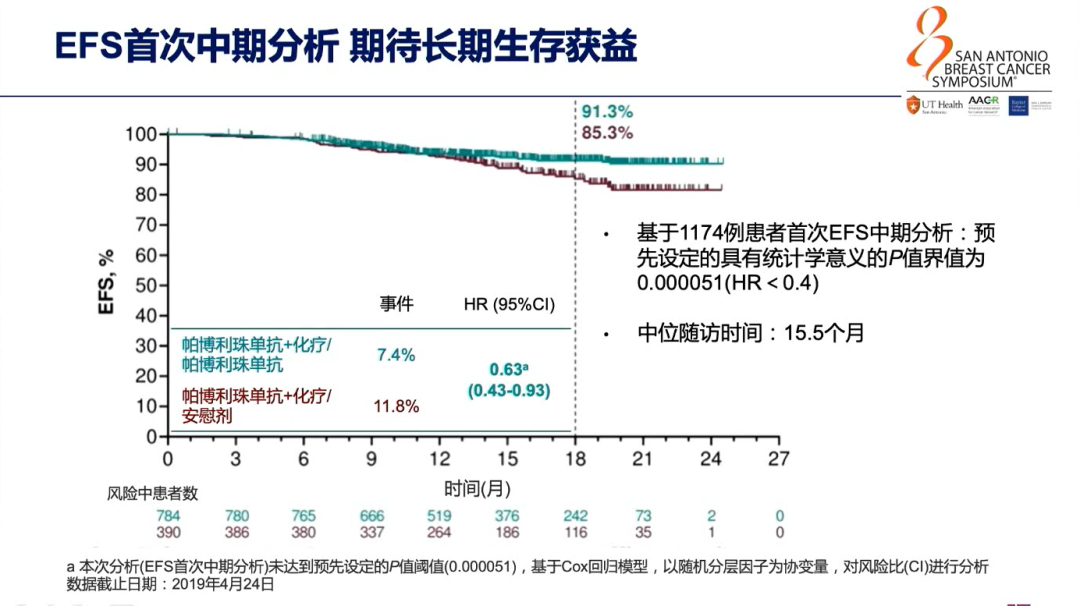
KEYNOTE-522研究是在早期TNBC新辅助治疗中应用帕博利珠单抗(Pembrolizumab)+化疗对比安慰剂+化疗后辅助治疗序贯帕博利珠单抗和安慰剂的Ⅲ期研究,入组患者为新诊断的T1c N1-2或T2-4 N0-2期、组织样本可供评估PD-L1检测的TNBC患者,主要研究终点是pCR(定义为ypT0/is ypN0)和无事件生存率(EFS)。基线人群中PD-L1阳性患者占到了81.6%和83.3%。该研究采用了目前TNBC最强的化疗方案(即卡铂+紫杉醇+多柔比星/表柔比星+环磷酰胺四药方案),分别配伍帕博利珠单抗或安慰剂。结果显示,帕博利珠单抗+化疗组pCR率显著高于安慰剂+化疗组(64.8% vs 51.2%,P=0.00055)。此外,研究者还发现无论PD-L1阳性/阴性患者都可以在新辅助治疗中有pCR的获益。EFS首次中期分析未能达到预先设定具有统计学意义p值的边界,但经过18个月的随访,IDFS绝对获益达到6%(91.3% vs 85.3%),虽然该研究数据尚未成熟,但是我们从中看到了获益趋势。
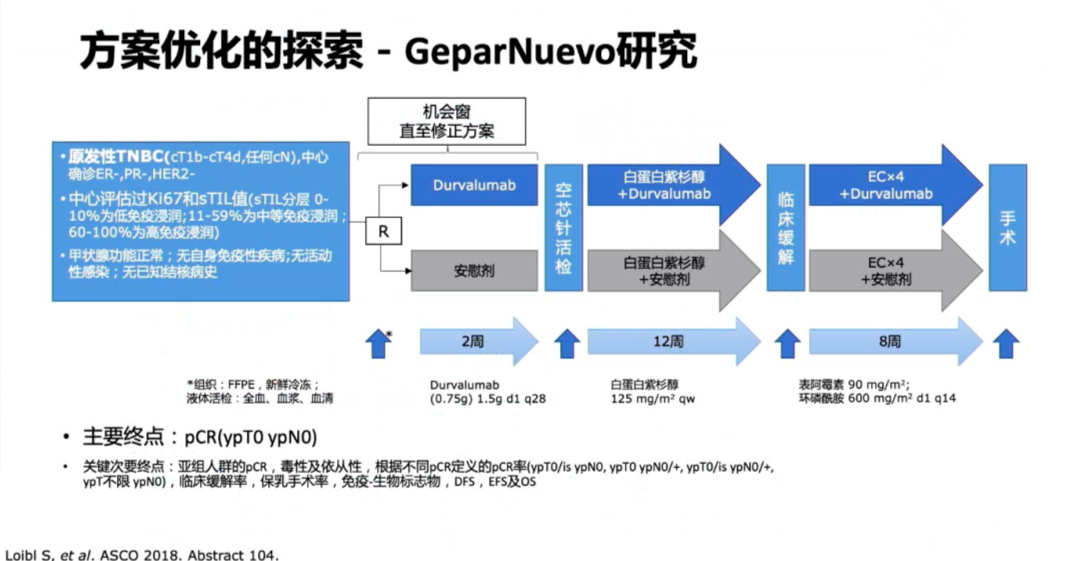
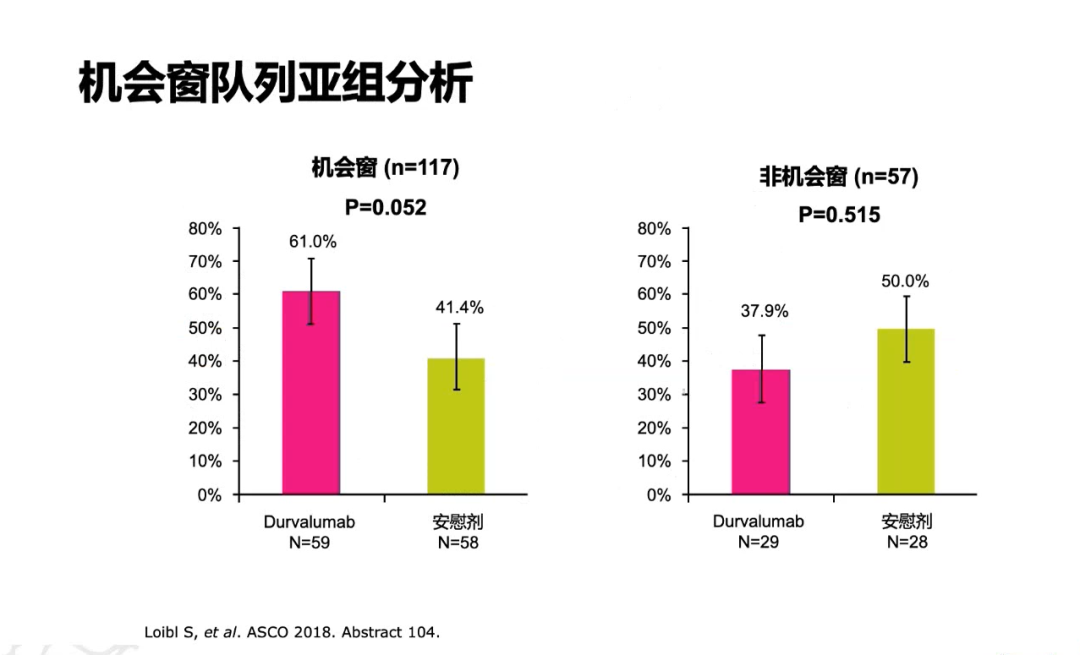
为探索何种配伍能够达到免疫治疗最好的疗效,研究者设计了GeparNuevo研究,该旨在探讨原发性TNBC(cT1b-cT4d,任何cN)患者中,紫杉序贯蒽环新辅助化疗的基础上联合抗PD-L1单抗Durvalumab的疗效。整体上患者pCR率没有显著差异(53.4% vs 44.2%,P=0.287),但预设的亚组分析,机会窗的患者(先在前2周接受Durvalumab或安慰剂单药治疗,然后进行空芯针活检并后续随机)与安慰剂相比,接受Durvalumab治疗的机会窗队列患者pCR率在数值上有明显提高(61.0% vs 41.4%,P=0.052)。该研究提示,未来可以选择化疗药物和免疫检查点抑制剂不同顺序的诱导治疗或选择不同化疗药物进行配伍的优化治疗方式。
除此之外,还可以尝试联合EGFR抑制剂、抗血管生成药物等,参照CREATE-X的研究模式,已有研究在评估新辅助治疗non-pCR的患者应用nivolumab+卡培他滨进行强化治疗的疗效。
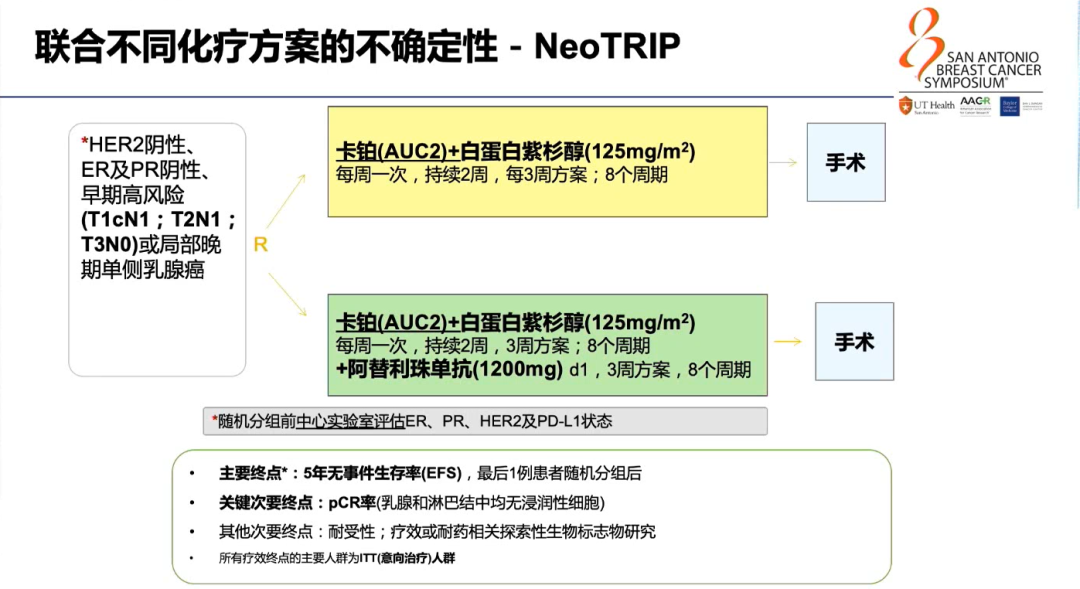
目前很多研究在探索有效的免疫治疗联合方案,NeoTRIP研究入组了HER2-、ER及PR-、早期高风险(T1cN1;T2N1;T3N0)或局部晚期单侧乳腺癌患者,采用化疗(白蛋白紫杉醇+卡铂)±阿替利珠单抗治疗。但在总体人群以及PD-L1阳性或阴性人群中,疗效并无显著提高,pCR率无差别。分析该阴性结果的原因可能是入组人群临床特征较为高危、病期较晚(淋巴结阳性占比高达87%)以及试验设计选用的化疗方案没有起到将“冷肿瘤”转变为“热肿瘤”的免疫诱导作用。
不同于细胞毒药物及内分泌治疗的作用机制,免疫治疗针对宿主,因此免疫治疗相关不良反应可能影响患者所有器官。不同的免疫治疗相关研究中不良反应谱并不一致,虽然整体上相对可控,但是粒缺性发热,免疫治疗相关肺炎等严重不良事件还占有相当的比例,且免疫治疗所致甲状腺功能异常也是非常常见,需要给予重视和干预。
由于作用机制的不同,在新辅助治疗中取得的pCR以及晚期治疗中的ORR能否转化为远期生存的获益呢?鉴于POPLAR研究、CHECKMATE-057研究以及CHECKMATE-025研究的PFS与OS结果并不一致,因此如何确定合理的治疗终点也是目前值得关注的问题。
总之,免疫治疗为早期TNBC的新辅助治疗带来机遇和挑战,希望今后能通过更多的研究进行探索,为TNBC带来更多治愈的机会。
《肿瘤瞭望》:免疫治疗已经改变了多种肿瘤传统的治疗模式,为恶性肿瘤患者带来新的希望。TNBC进展快、预后差且缺少特异性治疗手段,免疫治疗是TNBC探索的方向。越早应用,ORR越高,您如何看待早期TNBC的免疫治疗?
王殊教授:多项研究已在TNBC中进行了免疫治疗的尝试,结果陆续公布。如晚期一线的IMpassion 130研究,首次证实了转移性TNBC能够从抗PD-1抗体阿替利珠单抗免疫治疗中获益。新辅助治疗领域的KEYNOTE 522研究是评估在含有蒽环、紫杉和铂类的强势化疗基础之上加入帕博利珠单抗辅助治疗早期TNBC的Ⅲ期研究。IMpassion 031是在标准蒽环和紫杉基础之上加入阿替利珠单抗进行治疗的研究。两项研究都让我们看到了pCR率的显著提升,虽然远期生存的数据尚不成熟,但是就目前的趋势来看很有可能会得到阳性的结果。临床前研究和最近的临床研究结果值得我们对TNBC的免疫治疗从晚期前移到早期治疗持乐观态度。
《肿瘤瞭望》:早期的免疫检查点抑制剂单药的临床试验中,大部分患者疗效欠佳,引发了对免疫治疗耐药及可能的逆转策略的探讨。您如何看待提高免疫治疗反应率的问题?
王殊教授:与其他抗肿瘤治疗的作用机制不同,免疫治疗是通过增强宿主免疫系统来主动抵抗肿瘤的治疗方式,免疫检查点抑制剂包括抗细胞毒T淋巴细胞相关抗原4(CTLA-4)和抗PD-1/ PD-L1的单克隆抗体。尽管TNBC缺乏明确的治疗靶点,但是经过治疗后的肿瘤其通路会发生改变,这些改变有可能成为治疗的靶点。
?
由于肿瘤存在异质性,类似HER2阳性乳腺癌,单纯应用抗HER2治疗效果不佳,需要和化疗联合才能发挥最大疗效,单纯的免疫治疗的疗效其实也并不突出。目前免疫治疗多于化疗、靶向治疗(曲妥珠单抗、CDK4/6抑制剂、PARP抑制剂)、局部消融治疗联合以期提高缓解率。TNBC虽然作为免疫原性较高的一个分子分型,但是对免疫治疗仍然存在较大的异质性,通过检测如TILs等预测免疫治疗疗效和判断预后的指标,将有助于提升免疫治疗的疗效,但尚需更多的数据确认。未来发展趋势就是寻找与其他药物的最佳联合方案及适用人群。
医学博士,主任医师
现任北京大学人民医院乳腺中心主任、博士生导师
中国临床肿瘤学会乳腺癌专业委员会(CSCO-BC)常委
中国抗癌协会乳腺癌专业委员会(CBCSG)常委
中华医学会外科学分会乳腺学组委员
中国医师协会乳腺疾病专业委员会常委兼秘书长





 京公网安备 11010502033352号
京公网安备 11010502033352号